甲醇裂解制氢装置
氢气的应用
氢气的应用领域很大,主要应用于石油化工、电子工业、冶金工业、食品工业、浮法玻璃、精细有机合成、航天航空工业等领域。
常用制氢方式对比
常用制氢 方式有:天然气制氢、甲醇制氢、水电解制氢、氨分解制氢、燋炉煤气、氯碱气制氢等。各制氢方式优缺点对比:
| 比较项目 | 天然气制氢 | 甲醇裂解制氢 | 水电解制氢 |
氨分解制氢 |
| 技术成熟性 | 成熟 | 成熟 | 成熟 | 成熟 |
|
一次性投入 |
高 | 低 | 较高 | 低 |
|
生产成本 (元·Nm³) |
1~1.3 | ≤2.5 | 5~6 | 4~5 |
|
使用规模 (Nm³/h) |
>2000 | 20~2000 | 2~300 | 2~300 |
| 最高纯度% | 99.999 | 99.9997 | 99.999 | 99.99 |
| 杂质种类 | CO2、CO、CH4 | CO2、CO | O2、H2O | N2、NH3 |
| 建设地点 | 受限 | 自由 | 自由 | 受限 |
| 主装置占地 | 大 | 较大 | 较大 | 小 |
甲醇裂解制氢技术介绍
本工艺以来源方便的甲醇和脱盐水为原料,在220~280℃下,专用催化剂上催化转化为组成为主要含氢和二氧化碳转化气,其原理如下:
主反应: CH3OH=CO+2H2 +90.7 KJ/mol
CO+H2O=CO2+H2 -41.2 KJ/mol
副反应: 2CH3OH=CH3OCH3+H2O -24.9 KJ/mol
CO+3H2=CH4+H2O -+206.3KJ/mol
总反应: CH3OH+H2O=CO2+3H2 +49.5 KJ/mol
上述反应生成的转化气经冷却、冷凝后其组成为:
H2 73~74%
CO2 23~24.5%
CO 0~1.0%
CH3OH ≤300ppm
H2O 饱和
该转化气很容易用变压吸附等技术分离提取纯氢
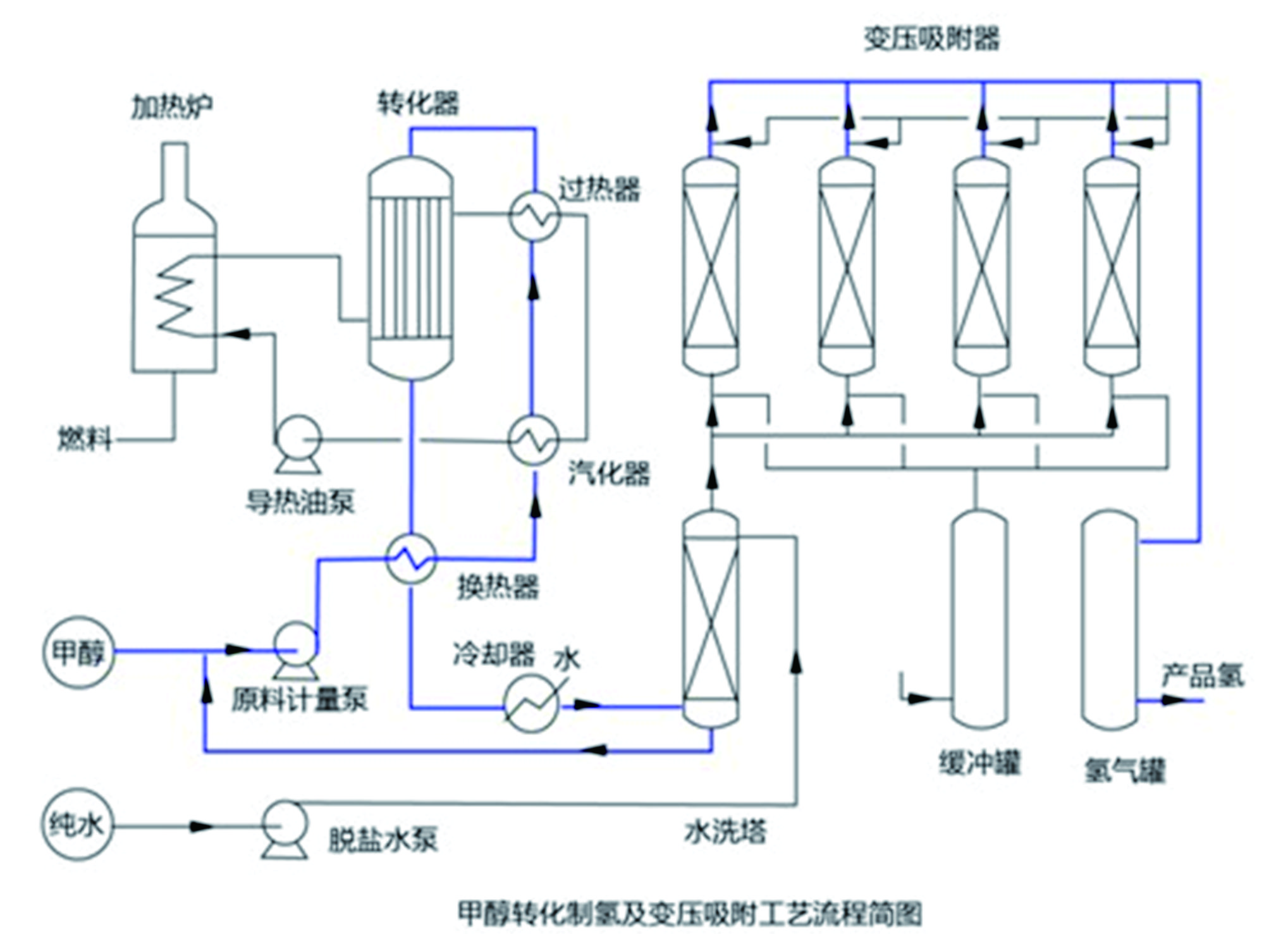
变压吸附分离制氢,该过程是将净化后转化气通过吸附剂并分离 出杂质组分CO2、CO的过程。其原理是利用吸 附剂对不同吸附质的选择性和吸附剂对吸附质 的吸附容量、压力变化有差异的特性,在高压下 吸附原料中的杂质组分,低压下脱附这些杂质而 使吸附剂获得再生,此工艺过程采用程序控制系 统进行自动化控制,改变操作条件可获得不同纯 度的氢气,纯度可达99.999%以上。
分子筛对一般气体分子的吸附顺序:
H2 < N2 < CH4 < CO < CO2
甲醇裂解制氢工艺特点
1.甲醇蒸汽在专用催化剂上裂解和转化一步完成;
2.采用加压操作,产生的转化气不需要进一步加压,即可直接送入变压 吸附分离装置,降低了能耗;
3.与电解法相比,电耗下降90%以上,生产成本可下降40~50%, 且氢气纯度高。与煤造气相比则显本工艺装置简单,操作方便稳定。煤造气 虽然原料费用稍低,但流程长投资大,且污染大,杂质多,需脱硫净化等, 对中小规模装置不适用;
4.专用催化剂具有活性高、选择性好、使用温度低,寿命长等特点;
5.采用导热油作为循环供热载体,满足了工艺要求,且投资少,能耗低,降低了操作费用。
甲醇制氢主要技术指标
原料消耗:
甲 醇:0.58~0.68 kg/m3H2
脱盐水:0.33~0.5 kg/Nm3H2
电 :≤0.1 kW/m3H
仪表空气:
种 类:空气
质 量:无油,露点≤-40℃
用 量:20~30Nm3/h
压 力:0.5~0.8MPa
循环水:
水 质:软化水
温 度:≤32℃
压 力:0.2~0.4MPa
导热油炉燃料消耗:
天燃气:0.2 Nm3 / Nm3H2
柴 油:0.2Kg / Nm3H2
液化汽:0.065Kg / Nm3H2
电加热:1.6-1.8KW / Nm3H2
分解气指标:
氢 气:约74%
二氧化碳:≤25%
一氧化碳:≤1%
甲 烷:微量
产品氢气指标:
产 量:50~10000Nm3/h
纯 度:≥99.9~99.9995% (V/V)
杂质含量(以纯度为99.999%)
如下: 一氧化碳:≤ 3ppm
二氧化碳:≤ 3ppm
甲 烷:≤ 1ppm





